Vert malachite
Le vert de malachite est un produit chimique toxique essentiellement réputé pour ses qualités de colorant bleu-vert.
Recherche sur Google Images :
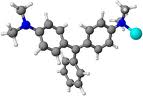
Source image : fr.academic.ru Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Page(s) en rapport avec ce sujet :
- ... Le vert de malachite (ou Vert Malachite) est une teinture organique qui se... Dû à ses propriétés antifongiques ainsi qu'à son faible coût, ... (source : wiki.aquatribu)
- ... Mais il possède d'autres propriétés telles que le traitement des parasites ou des infections. Pour finir le vert malachite est particulièrement utilisé... (source : oboulo)
- Grand vase vert malachite soufflé à la bouche "La danse". €249. Ce superbe et grand vase vert malachite est en verre soufflé à la bouche, sablé et poli... (source : shopmania)
| Vert malachite | |
|---|---|
 |
|
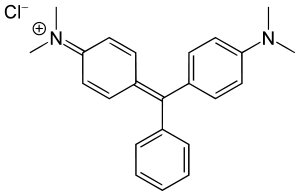
| Structure du vert Malachite | |
| Général | |
| Nom IUPAC | 4-[ (4-dimethylaminophenyl) -phenyl-methyl]- N, N-dimethyl-aniline |
| Synonymes | C. I. 42000 C. I. Basic Green 4 |
| No CAS | (cation) (HCl) (oxalate) |
| No EINECS | |
| Apparence | cristaux vert foncé |
| Propriétés chimiques | |
| Formule brute | C23H25ClN2 [Isomères] (sel) |
| Masse molaire[1] | 364, 911 ± 0, 023 g·mol-1 C 75, 7 %, H 6, 91 %, Cl 9, 72 %, N 7, 68 %, |
| pKa | pKa1 : 1, 3 pKa2 : environ 12, 5 |
|
|
|
Le vert de malachite (ou vert d'aniline, ou vert de diamant B) est un produit chimique toxique essentiellement réputé pour ses qualités de colorant bleu-vert.
Il a aussi été utilisé pour traiter les parasites, les infections fongiques, et les infections bactériennes dans le poisson et les œufs de poisson. Il possède aussi des propriétés bactériologiques.
Cependant, en 1992, au Canada, on a montré qu'il existait un risque sanitaire significatif pour les humains qui ont mangé des poissons contenant du vert de Malachite et le composé a été répertorié en classe II. Il s'est avéré que la molécule était toxique pour les cellules humaines et qu'il existait une possibilité qu'elle soit la cause de la formation de tumeurs au foie. Cependant, à cause de sa facilité de préparation et du faible coût de sa synthèse, il est toujours employé dans certains pays avec des lois moins restrictives ne concernant pas l'aquaculture. En 2005, des anguilles et des poissons importés de Chine ont été trouvés à Hong Kong avec des traces de ce produit chimique.
La solution aqueuse du vert Malachite a un goût un peu amer. Une bonne manière d'enlever la teinture des dents est de les rincer avec une solution d'éthanol.
Enfin, les dernières caractéristiques intéressantes du vert Malachite sont ses propriétés d'indicateur coloré de pH en chimie. Le vert Malachite possède deux zones de virages, un en milieu particulièrement acide et un en milieu particulièrement basique.
Le nom de «Vert de Malachite» provient du nom d'un carbonate minéral : la Malachite.
Structure du Vert Malachite
Propriétés acido-basiques
Le vert de Malachite est utilisé comme indicateur coloré dans les dosages acido-basiques en chimie. Il possède trois formes différentes caractérisées par différentes couleurs qui permettent de déterminer le pH d'une solution.
| Couleurs du vert de Malachite | forme acide jaune |
zone de virage 1 pH 0.2 à pH 1, 8 |
forme classique bleu-vert |
zone de virage 2 pH 11.5 à pH 13.2 |
forme basique incolore |
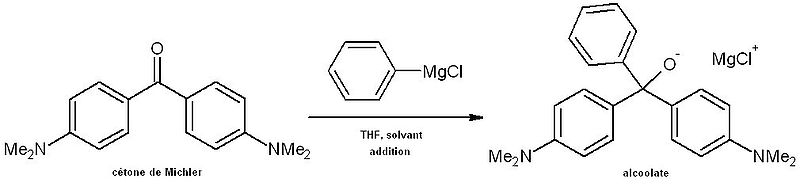
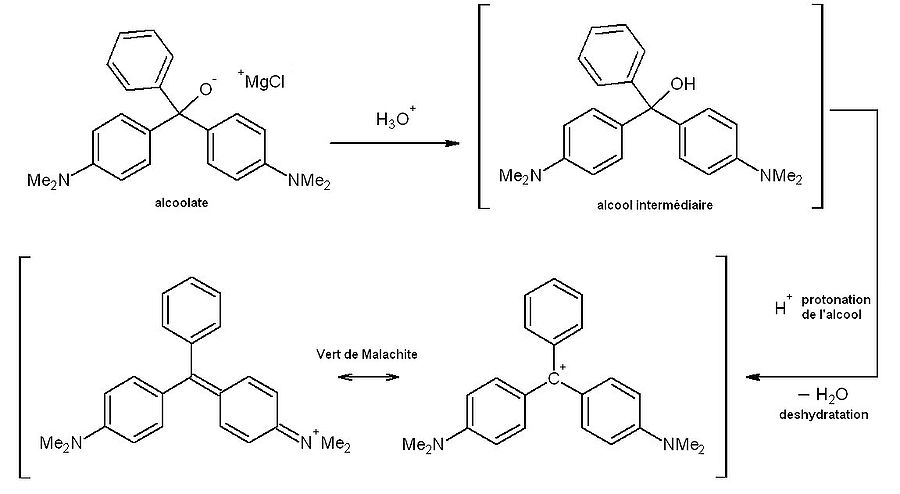
Synthèse du vert de Malachite[2].
L'addition d'un réactif de Grignard (ici le chlorure de phényl magnésium C6H5MgCl) sur la cétone de Michler (ou 4, 4'-bis (diméthylamino) -benzophénone (Me2NPh) 2CO) conduit à l'obtention d'un alcoolate tertiaire intermédiaire.
Dans un second temps, une hydrolyse en milieu acide fort (HCl 1N) conduit à l'alcool tertiaire intermédiaire. Ce dernier se déshydrate spontanément au sein du mélange réactionnel formant le carbocation stable, soluble dans le l'eau. Le vert de Malachite est stabilisé par mésomérie.
Notes et références
- Masse molaire calculée selon Atomic weights of the elements 2007 sur www. chem. qmul. ac. uk
- Sabine Chierici, Fascicules de TP de chimie organique de l'UE CHI232 "Chimie expérimentale", UJF, 2006
Lien externe
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 30/11/2010.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité